أسئلة المحتوى وإجاباتها
التفاعلات الكيميائية
أفكر صفحة (87):
أي الشكلين الآتيين يمثل تفاعلاً كيميائياً؟ أفسر إجابتي.
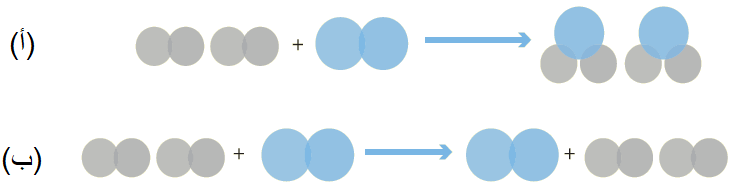
الشكل (أ) يمثل تفاعلاً كيميائياً؛ لأنه نتج عنه مواد جديدة تختلف عن المواد المتفاعلة.
أتحقق صفحة (88):
يتفاعل عنصر المغنيسيوم الصلب مع غاز الكلور، وينتج كلوريد المغنيسيوم الصلب، أكتب معادلة كيميائية لفظية ومعادلة كيميائية رمزية تعبر عن هذا التفاعل.
المعادلة اللفظية:
مغنيسيوم + غاز الكلور ← كلوريد الصوديوم
المعادلة الرمزية:
Mg(s) + Cl2(g) → MgCl2(s)
أتحقق صفحة (90):
أزن المعادلة الكيميائية الآتية:
Na(s) + Cl2(g) → NaCl(s)
2Na(s) + Cl2(g) → 2NaCl(s)
أتحقق صفحة (93):
أكتب معادلة كيميائية موزونة تمثل التفاعل الحاصل بين الليثيوم والأكسجين.
ليثيوم + غاز الأكسجين ← أكسيد الليثيوم
4Li(s) + O2(g) → 2Li2O(s)
تجربة صفحة (94):
تفاعل الفلزات مع الأكسجين
التحليل والاستنتاج:
1- أفسر سبب الاختلاف بين المواد في التفاعل الكيميائي.
المتفاعلات: المغنيسيوم فلز لامع، والأكسجين غاز.
النواتج: أكسيد المغنيسيوم صلب لونه أبيض.
اختلفت المواد المتفاعلة عن المواد الناتجة؛ بسبب حدوث تفاعل كيميائي.
2- أكتب معادلتي التفاعل الكيميائي: اللفظية والرمزية.
المعادلة اللفظية:
مغنيسيوم + غاز الأكسجين ← أكسيد المغنيسيوم
المعادلة الرمزية:
Mg(s) + O2(g) → MgO(s)
3- أزن معادلة التفاعل اللفظية والرمزية.
2Mg(s) + O2(g) → 2MgO(s)
أفكر صفحة (95):
يحفظ البوتاسيوم مغموساً في الكيروسين أو زيت البرافين، لماذا؟
لمنع وصول أكسجين الهواء والماء إلى البوتاسيوم؛ لأن البوتاسيوم شديد التفاعل مع الأكسجين والماء.
أتحقق صفحة (95):
أكتب معادلة كيميائية موزونة للتفاعل الحاصل بين المغنيسيوم والماء.
مغنيسيوم + ماء ← هيدروكسيد المغنيسيوم + غاز الهيدروجين
Mg(s) + 2H2O(l) → Mg(OH)2(aq) + H2(g)
أفكر صفحة (96):
لماذا ينصح بتهوية الغرف التي تستخدم فيها المدافىء التي تعمل باستخدام الكاز في فصل الشتاء؟
احتراق الكاز (الوقود) ينتج غاز ثاني أكسيد الكربون، وفي حال نقص الأكسجين في الغرفة ينتج عن احتراق الكاز غاز أول أكسيد الكربون، وهو غاز سام؛ ما يسبب الاختناق، لذا يجب تهوية الغرفة باستمرار.
أتحقق صفحة (96):
أحدد بعض الخصائص الفيزيائية للافلزات.
- رديئة التوصيل للكهرباء والحرارة.
- غير قابلة للسحب والطرق.
- معظمها غازية في درجة حرارة الغرفة، وبعضها صلبة هشة أو سائلة.
تجربة صفحة (97):
تفاعل اللافلزات مع الأكسجين
التحليل والاستنتاج:
1- أفسر سبب الاختلاف بين المواد في التفاعل.
المتفاعلات: الكبريت صلب هش لونه أصفر، والأكسجين غاز.
النواتج: أكسيد الكبريت غاز.
اختلفت المواد المتفاعلة عن المواد الناتجة؛ بسبب حدوث تفاعل كيميائي.
2- أستنتج الأدلة على حدوث تفاعل كيميائي.
تغير لون الكبريت الأصفر.
تغير لون ورقة تباع الشمس المبللة بالماء عند غمسها بالناتج.
3- أكتب معادلتي التفاعل: اللفظية والرمزية.
المعادلة اللفظية:
كبريت + غاز الأكسجين ← أكسيد الكبريت
المعادلة الرمزية:
S(s) + O2(g) → SO2(g)
4- أتوقع تأثير المادة الناتجة، أهو حمضي أم قاعدي؟
تأثير SO2 حمضي.
إعداد : شبكة منهاجي التعليمية
04 / 04 / 2025
النقاشات