 |
الطلاء الكهربائي
Electroplating
الطلاء الكهربائي: ترسيب طبقة رقيقة من ذرات فلز يُراد الطلاء به على سطح فلزٍ آخر لحمايته من المؤثرات الخارجية وإعطائه مظهراً جمالياً، باستخدام عملية التحليل الكهربائي.
الهدف من الطلاء الكهربائي:
- حماية الفلزات من التآكل ومن المؤثرات الخارجية.
- إكساب الفلز مظهراً جمالياً.
أمثلة على الطلاء الكهربائي:
- طلاء هياكل السيارات.
- طلاء الأدوات المنزلية.
- طلاء المفاتيح والمجوهرات التقليدية.
خطوات الطلاء الكهربائي:
- يربط الفلز المراد طلاؤه بالقطب السالب لمصدر التيار (المهبط).
- تربط قطعة من الفلز المراد الطلاء به بالقطب الموجب لمصدر التيار (المصعد).
- يغمس القطبان بمحلولٍ ملحي لمادة الطلاء (من مادة المصعد).
خطوات طلاء ملعقة من الحديد بطبقة من الفضة:
- تنظف الملعقة جيداً للتأكد من عدم وجود مادة دهنية عليها.
- تربط الملعقة بسلك ويربط مع القطب السالب لبطارية (المهبط).
- تربط قطعة من الفضة بسلك ويربط مع القطب الموجب لبطارية (المصعد).
- تُغمر الملعقة وقطعة الفضة بمحلول نترات الفضة أو أي ملح ذائب يحتوي على أيونات الفضة.
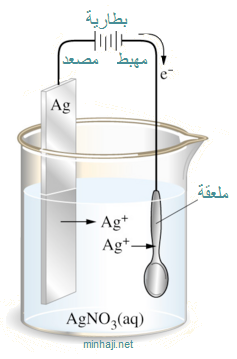
مبدأ الطلاء الكهربائي:
- تتجه أيونات الفضة +Ag في المحلول إلى القطب المعاكس لها في الشحنة وهو القطب السالب (المهبط) ويمثله الملعقة في هذه الخلية، وتتعرض للاختزال وتتحول إلى ذرات فضة تترسب على الملعقة.
- تتعرض ذرات المصعد (قطعة الفضة) للتأكسد، وتتحول ذراتها إلى أيونات تنتقل إلى المحلول.
المعادلات التي تحدث على كلّ قطب:
Ag+ + e- → معادلة المصعد Ag
Ag → معادلة المهبط Ag+ + e-
سؤال:
إذا أردت طلاء قطعةٍ من الحديد بطبقةٍ من الخارصين فأجب عن الأسئلة الآتية في ضوء دراستك لهذه العملية:
- اقترح محلولاً ملحياً يمكن استخدامه في خلية الطلاء الكهربائي.
- أيهما يشكل المصعد الحديد أم الخارصين؟
- اكتب التفاعلات التي تحدث عند كل قطبٍ.
الإجابة:
- محلول أحد أملاح الخارصين، مثل كبريتات الخارصين ZnSO4
- الخارصين هو المصعد.
- التفاعلات:
Zn2+ + 2e → Zn معادلة المصعد
Zn → Zn2+ + 2e معادلة المهبط